La técnica de citometría de flujo hace referencia a la medida o análisis (metría) de células (cito) en movimiento (flujo). Consiste, por tanto, en una medida continua e individual de parámetros celulares en una suspensión de células mantenidas en una corriente líquida. Dicha técnica se realiza en un aparato que recibe el nombre de citómetro de flujo (FACS, del inglés Fluorescence-activated cell sorter).
En primer lugar, el fluido de muestra se inyecta en la parte central del sistema de fluidos del citómetro de flujo. A continuación, se produce una corriente de partículas que atraviesan el núcleo del compartimento una por una, con el objetivo de poder analizarlas de manera individual, lo que se conoce como enfoque hidrodinámico. Seguidamente, se encuentra un láser que se utiliza como principal fuente de luz en el citómetro.
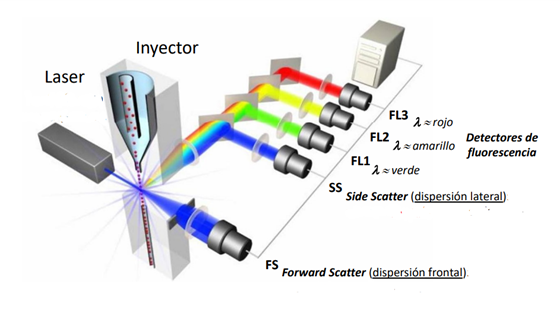
Como se ha mencionado anteriormente, estas partículas pasan de forma individual, atravesando el haz del láser cada una de ellas por un punto, llamado punto de interrogación. La luz es dispersada por cada una de las partículas que pasa por dicho punto, y puede medirse con dos detectores diferentes:
- Forward scatter (FSC, dispersión frontal): detecta la luz dispersada por las células hacia delante y da información sobre el tamaño de la partícula.
- Side scatter (SSC, dispersión lateral): detecta la luz dispersada por las células a 90° de la línea de propagación del láser, y da información sobre la complejidad interna y la granularidad de la partícula.
Por último, la señal detectada cuando pasa la partícula por el punto de interrogación se convierte en un pulso eléctrico que es recogido por el detector.
¿Qué se puede detectar gracias al citómetro de flujo?
Los fluoróforos son marcadores fluorescentes que se utilizan para detectar la expresión de moléculas celulares como pueden ser proteínas. Existen diferentes tipos de fluoróforos (FITC, PE, APC…) en función del experimento. Gracias al marcaje con estos fluoróforos se pueden diferenciar subpoblaciones de células y estudiar una gran variedad de procesos celulares.
¿Qué datos se obtienen de un análisis por citometría de flujo?
El análisis de datos de la citometría de flujo se basa en el principio del sistema de ventanas (gating), donde cada punto que aparezca en el gráfico representará una célula individual que ha atravesado el láser. Los datos recogidos por el citómetro de flujo pueden analizarse mediante dos tipos de gráficos diferentes:
Histogramas univariantes (Figura 2), donde se representa un parámetro relativo a la fluorescencia en el eje de abscisas y el número de células en el eje de ordenadas. Los datos que se expresan en el histograma pueden ser todos los datos obtenidos o de una población previamente seleccionada.

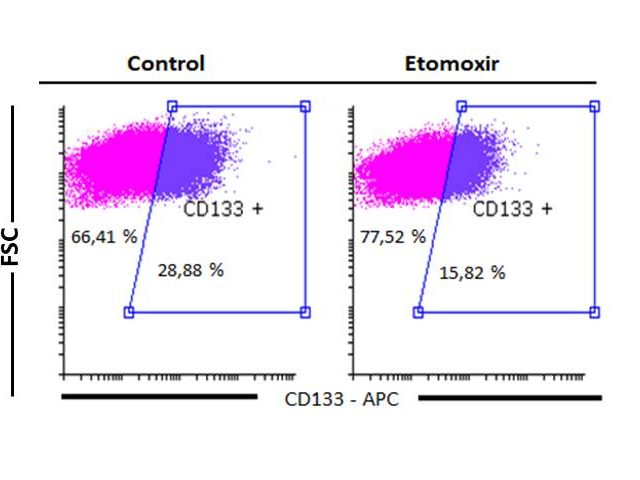
Por otro lado, están los histogramas bivariados donde se analizan dos parámetros de medición, uno en el eje de las abscisas y otro en el de ordenadas. Las células se muestran como un gráfico de densidad (density plot, Figura 3) o de puntos (dot plot, Figura 4).

¿Para qué aplicaciones se puede utilizar la citometría de flujo?
Los marcadores fluorescentes son muy útiles en una amplia gama de aplicaciones, ya que permiten el estudio de propiedades biológicas y bioquímicas de un antígeno de interés. La ventaja que tiene la citometría de flujo es que un único láser puede excitar varios fluoróforos, y mediante el uso de filtros es posible analizar varios parámetros de interés de la muestra.
Entre algunas de las aplicaciones más utilizadas se encuentran:
– Inmunofenotipado: se basa en la identificación de marcadores en las células del sistema inmunitario. Se pueden identificar diferentes tipos celulares gracias al uso de distintos marcadores. Además, esta aplicación se utiliza en la clínica para el diagnóstico de enfermedades.

– Apoptosis: es uno de los procesos celulares con gran interés en la citometría de flujo, ya que permite separar las células en función de la fase apoptótica en que se encuentren. Uno de los marcadores más utilizados es la Anexina V conjugada con un fluoróforo.
– Proliferación/ciclo celular: se puede realizar la tinción de las células con un anticuerpo contra un marcador de proliferación celular como puede ser el Ki67, MCM2 o PCNA. Otro método es la incubación de las células con BrdU que tiene la capacidad de incorporarse al ADN durante la fase S del ciclo celular.

De hecho, para nosotros en el laboratorio se trata de una técnica de rutina. Por ejemplo, al trabajar con tumores humanos implantados en ratones, el marcador hEpcam nos permite determinar el porcentaje de células epiteliales humanas presentes en estos. Además, gracias a la citometría de flujo somos capaces de separar las células tumorales en dos subpoblaciones celulares, las CD133+ (células madre tumorales) de las CD133– (células diferenciadas).
Por otro lado, también nos permite cuantificar parámetros metabólicos de las células de pacientes de cáncer de páncreas, como el contenido de gotas de grasa (LD540) así como los lípidos totales (Bodipy). Asimismo, se utiliza el marcador NBDG junto con LD540 y Bodipy para diferenciar las células según su metabolismo glucolítico vs lipogénico respectivamente.
Otra aplicación de gran uso gracias a la citometría en el laboratorio, es la cuantificación del porcentaje de muerte celular mediante la apoptosis (Anexina V), que nos permite evaluar si nuestros tratamientos matan las células madre tumorales, lo que es principal objetivo de nuestra investigación.
La citometría de flujo se trata por tanto de una herramienta muy potente para la investigación en diversos campos de estudio. Por ello, hoy en día tiene una gran utilidad en múltiples aplicaciones. Además, se caracteriza por ser una técnica que se ha vuelto mucho más accesible para los investigadores gracias a la reducción de la complejidad de los instrumentos, la automatización, el aumento de sensibilidad y diversos softwares fáciles de usar.
